程冬炳副研究员、孙涛垒教授联合国家纳米科学中心乔增莹研究员、王浩教授和哈尔滨医科大学徐万海教授使用治疗肿瘤方面有新突破
程冬炳副研究员、孙涛垒教授联合国家纳米科学中心乔增莹研究员、王浩教授和哈尔滨医科大学徐万海教授使用治疗肿瘤方面有新突破,该研究成果“In vivo assembly enhanced binding effect augments tumor specific ferroptosis therapy”发表在 《Nature commucation》(IF=16.6)上,孙涛垒教授、乔增莹研究员和王浩教授为通讯作者。
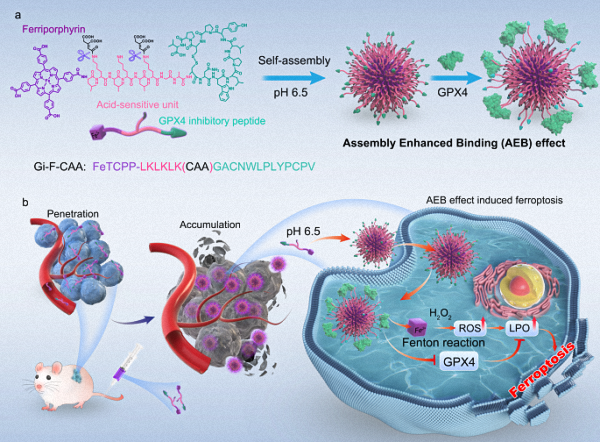
新的研究表明谷胱甘肽过氧化物酶 4 (GPX4) 抑制剂激活铁死亡可能是抑制肿瘤的重要治疗策略。然而,由于肿瘤递送效果差和铁死亡的非特异性激活,GPX4抑制剂在肿瘤治疗中的广泛应用受到阻碍。利用体内自组装的优势,我们开发了一种具有肿瘤微环境特异性激活功能的肽-铁卟啉缀合物,以改善肿瘤渗透、内吞作用和 GPX4 抑制,最终通过铁死亡增强其抗癌活性。简而言之,GPX4 抑制肽与用 pH 敏感部分和铁卟啉修饰的组装肽接头缀合,产生肽-铁卟啉缀合物 (Gi-F-CAA)。在肿瘤的酸性微环境下, CAA水解后疏水作用增强, Gi-F-CAA自组装成大纳米颗粒(Gi-F),提高肿瘤内吞效率。重要的是,Gi-F 通过组装增强结合 (AEB) 效应显着抑制 GPX4 活性,增强基于铁卟啉的芬顿反应的氧化应激,最终在多种肿瘤模型中实现抗肿瘤特性。我们的研究结果表明,这种具有AEB效应的肽-铁卟啉缀合物设计可以通过诱导铁死亡来提高治疗效果,为克服化疗耐药性提供替代策略。
文章信息:Dayong Hou, Dongbing Cheng, Niyuan Zhang, Zhijia Wang, Xingjie Hu, Xin Li, Meiyu Lv, Xiangpeng Li, Lingrui Jian, Jinpeng Ma, Taolei Sun*, Zengying Qiao*, Wanhai Xu, Hao Wang*. In vivo assembly enhanced binding effect augments tumor specific ferroptosis therapy[J]. Nature commucation, 2024, 15: 454.

